4. катализ и реакции на поверхности
4.1. Катализ ферментами
4.1.1. Напишите кинетическое уравнение для реакции
E + S ![]() ES1
ES1 ![]() ES2 …
ES2 … ![]() ESi
ESi ![]() P + E.
P + E.
4.1.2. Получите кинетическое уравнение для процесса
ферментативного катализа, в котором участвуют два промежуточных компонента:
E + S ![]() ES1
ES1 ![]() ES2
ES2 ![]() E +
P.
E +
P.
4.1.3. Реакция, катализируемая ферментом Е, протекает согласно следующей схеме
превращений:
E + S ![]() ES
ES ![]() E + P.
E + P.
Найдите
зависимость начальной скорости реакции от начальной концентрации субстрата,
если [E]t = 0
= Е0, [S]t = 0
= S0. Определите время достижения квазистационарного режима
протекания реакции.
4.1.4. Для реакции,
протекающей по механизму
![]() ,
,
![]()
![]() ,
,
найдите
зависимость начальной скорости реакции W от
начальной концентрации субстрата S.
4.1.5.
Каталитический
процесс S ¾® P осуществляется по механизму
|
1) S + E |
2) C1 + S |
3) C1 |
|
k1
= 102 M–1×c–1 k–1
= 10–1 c–1 |
k2/k–2 = 10 M–1 |
k3
= 10 c–1 |
Рассчитайте
максимальную скорость реакции при [E]0
= 10–6 M и варьируемой [S].
4.1.1.
Реакция
выделения водорода из воды под воздействием сильного восстановителя
катион-радикала метилвиологена (S)
катализируется ферментом гидрогеназой по схеме
S + E
![]() ES,
ES,
S + ES ![]() ES2
ES2
ES2 + 2 H+![]() E + 2 S+ + H2.
E + 2 S+ + H2.
Напишите
выражение для скорости выделения водорода и найдите порядок реакции по S, E
и Н+ при условии, что K1 = K2 = 1 M–1, pHисх = 2; [Е]0 = 1015 см–3;
[S]0 = 10–2 М.
Оцените
константу k3, зная, что из 100 мл раствора за час выделилось
2 мл H2 (P =
4.1.2. Разложение Н2О2 ферментом каталазой идёт по механизму
1) H2O2 + E ![]() C.
C.
2) C + H2O2 ![]() E + O2 + 2 H2O.
E + O2 + 2 H2O.
Одновременно
происходит термическая денатурация фермента, приводящая к полной потере им
каталитических свойств
3) E ![]() D.
D.
При
80 °С k1 = 1,2 × 107 М–1с–1, k2
= 8,5 × 107 М–1с–1, k3
= 3,15 с–1.
Какой
процент Н2О2 прореагирует к моменту
прекращения реакции из-за денатурации фермента при начальной концентрации
фермента СЕ0 = 1,5 × 10‑7 М при условии, что ![]()
![]() ?
?
4.1.3.
(П1–2005, №
1). Гидролиз нитрила миндальной
кислоты RCN в оптический R-изомер миндальной
кислоты RCOOH протекает в водном растворе в присутствии фермента нитрилазы (Е) по кинетической схеме:
RCN + E ![]() {RCN × E}
{RCN × E}
{RCN × E} + 2 H2O
![]() E + RCOOH + NH3
E + RCOOH + NH3
{RCN × E} ![]() C (дезактивация фермента).
C (дезактивация фермента).
В
реактор загрузили
4.1.4.
(КР3–2004,
№ 2). Реакция, катализируемая
ферментом E,
подчиняется схеме Михаэлиса – Ментен (KM =![]() 3 × 10–3 M):
3 × 10–3 M):
E + S ![]() ES
ES ![]() E + P.
E + P.
Присутствие
ингибитора I приводит к обратимой дезактивации фермента:
E + I ![]() EI
EI ![]() = 3 × 10–4 M.
= 3 × 10–4 M.
При
какой концентрации ингибитора скорость реакции уменьшится в два раза по
сравнению с неингибированной реакцией, если концентрация субстрата равна 3 × 10–3 M и [E]0 << [I], [S].
4.1.5.
(Экз–2005,
№ 3). Гомогенное каталитическое гидрирование этилпирувата (S) осуществляют в
водном растворе, пробулькивая через него водород при фиксированном давлении.
Предполагая, что концентрация этилпирувата
1) E + S ![]() ES
ES
2) H2 + 2 E ![]() 2 EH
2 EH
3) ES + EH ![]() EHS + E
EHS + E
4) EHS + EH ![]() H2S + 2 E
H2S + 2 E
значительно превышает концентрацию катализатора (E), по приведённой схеме реакции рассчитайте скорость гидрирования.
4.1.6.
(КР3–2007, №4). Оцените значения константы Михаэлиса KM и максимальной скорости гидролиза Wmax метилового эфира N-ацетил -L-норвалина,
катализируемого a - химотрипсином по механизму:
![]()
Данные по зависимости начальной скорости W0 от концентрации субстрата [S]0:
|
[S]0×102, M |
4,00 |
2,00 |
1,33 |
1,00 |
0,80 |
|
W0×107,
M с-1 |
10,0 |
7,85 |
6,51 |
5,51 |
4,80 |
4.1.7.
(КР3–2008, № 4). Гидролиз ацетилхолина ферментом холинэстеразой
осуществляется по механизму:
1) S + E 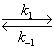 C, 2) C
C, 2) C ![]() P + E.
P + E.
При [S] = 2,5×10−4 M, [E]0
= 10−7 M скорость
реакции была равна 1,4×10−2 М×с−1. Спектральными методами установлено, что в
этих условиях 20% фермента находится в форме комплекса с ацетилхолином.
Определите величину k2 и константу Михаэлиса KМ.