 *
Зависимости
*
Зависимости
85. (3/1-94). В закрытый, предварительно вакуумированный сосуд поместили некоторое количество твердого NH4Cl, способного к обратимому разложению по реакции
NH4Cl(тв.) ↔ NH3(г)+ HCl(г).
После установления термодинамического равновесия в сосуде оказалось, что давление газа внутри него стало равным 2 атм.
Оцените температуру сосуда и изобразите качественно график P = P(Т) для дальнейшего нагревания сосуда.
| Вещество |
NH4Cl(тв) |
NH3(г) |
HCl(г) |
| ΔfHo298(кДж/моль) |
–314 |
–46 |
–92 |
| ΔSo298 (Дж/моль·К) |
96 |
193 |
187 |
86. (3/1-97). Рассчитать стандартную энтальпию образования,
QP
= –189 кДж/моль его разложения при стандартных условиях по реакции
NH4Cl O4(крист) = 0,5N2(газ) + 0,5Cl2(газ) + О2(газ) + 2Н2О(газ).
|
|
|
|
|
| Cl2(газ) |
0 |
233 |
34 |
| H2(газ) |
0 |
131 |
29 |
| H2O(газ) |
–242 |
189 |
34 |
| N2(газ) |
0 |
192 |
29 |
| NH3(газ) |
–46 |
193 |
35 |
| O2(газ) |
0 |
205 |
29 |
87. (4/Э-95). В два предварительно откачанных и помещенных в термостат сосуда, соединенных между собой трубкой, поместили раздельно СаСО3 и СаО. Что будет находиться в сосудах после установления термодинамического равновесия при температуре, достаточной для разложения карбоната? Как изменится результат, если: а) в обоих сосудах исходно находится чистый CaCO3; б) в сосуды исходно добавлен СО2? Соединения кальция можно считать нелетучими.
88. (5/Э1-94,99). Термическое разложение карбонатов двух различных металлов
MCO3= MO + CO2
описывается уравнениями
lg KP1 = –9000/T + 2,0, (1)
lg KP2 =–3000/T + 3,0. (2)
В вакуумированный и термостатированный при 1000 К сосуд объемом 10 л вносится по 0,01 моля каждого карбоната. Определите состав системы после ее прихода в равновесие. Как изменится ответ, если исходно сосуд не был вакуумирован?
89. (5/1-04) В вакуумированный сосуд объемом 22,4 л поместили по 0,1 моля CaCO3 и BaCO3 и нагрели до 1000 К. Определить равновесный состав системы, если известна температурная зависимость констант равновесия Кр в интервале 900 – 1000 К для процессов:
СаСО3(тв) = СаО(тв) + СО2(г); ln KP = – 20489/>T + 17,74;
ВаСО3(тв)= ВаО(тв) + СО2(г); ln KP = – 34381/T + 23,15.
90. (5/1-97). В вакуумированный сосуд объемом 32,8 л поместили по 1 молю CaO и PbCO3 и нагрели до 800 К. Найти равновесный состав (PCO2, атм и количества твердых компонентов, моль), если известна температурная зависимость констант равновесия K P для процессов:
(1) CaCO3(тв) = CaO(тв) + CO2(газ); lgK1 = –8000/T + 10,0;
(2) PbCO3(тв) = PbO(тв) + CO2(газ); lgK2 = –6000/T + 8,0.
Как изменится равновесный состав системы, если вместо CaO взять 1 моль CaCO3, а вместо PbCO3 – 1 моль PbO?
Оценить, при каких температурах возможна твердофазная реакция
CaCO3 + PbO = CaO + PbCO3,
если известно, что указанные оксиды и карбонаты не образуют твердых растворов.
91. (4/1-03). В исходно вакуумированный герметичный термостатированный сосуд с поршнем, под которым поддерживается постоянное давление 1 атм, поместили по 1 молю твердых веществ А и С, способных к разложению по реакциям:
А(тв)=B(газ) +A’(тв); KP1=1 бар;
C(тв)= D(газ)+C’(тв); KP2=3 бар.
Известно, что вещества В и D способны реагировать в газовой фазе по реакции
В + D = Е KP3 = 3 бар–1.
Определить состав (в молях) равновесной газовой смеси под поршнем. Как изменится ответ, если в сосуде под поршнем исходно находился также инертный газ под давлением 1атм?
92. (4/1-00). В химических циклах переработки плутония используется перевод этого элемента в газообразное соединение по реакции с молекулярным фтором при 300° C:
PuF4(тв) + F2(г) = PuF<6(г).
Каков равновесный состав (мол. %) газа после прохождения такой реакции, если общее давление газа 1 бар, а значение Кр = 26,6 ·10–4? Сколько молей F2 необходимо ввести в реактор для получения 1 г PuF6 в этих условиях? Атомная масса Pu – 244, F – 19.
93. (6/1-00). В адиабатической оболочке при 980 К и давлении 1 бар находится 1 моль кристаллического вещества А, для которого в определенных условиях возможно превращение в кристаллическое вещество В. Стандартные энергии Гиббса этих веществ, не способных к образованию твердых растворов, описываются уравнениями
GA = 81000 – 25T – 25TlnT,
GB = 80000 – 24T – 25TlnT.
Опишите равновесное состояние системы (температуру и равновесный состав).
94. (3/1-02). Стандартная энергия реакции дегидратации соли MX2H2(тв) = MX2(тв) + H2O(газ) описывается уравнением
Δ DrGo= 36170,7 – 68,514 T, Дж/моль.
В первый реакционный сосуд помещают 1 моль моногидрата и 1 моль безводной соли, во второй – 1,2 моля безводной соли. Сосуды соединяют трубкой и нагревают: первый – до температуры 500 К, второй – до температуры 490 К. Кроме того, обе формы соли во втором сосуде механически сжимают до давления 500 бар. Общий объем газовой фазы, не занятой реагентами, равен 0,12 л. Мольные объемы безводной формы соли и моногидрата равны 40,02 см3 и 56,89 см3 соответственно. Опишите конечное состояние системы.
95. (6/1-01). Кристаллогидраты (M1)SO4· 6 H2O и (M2)SO46· H2O способны к дегидратации:
(M1)SO4· 6 H2O = (M1)SO4· 4 H2O + 2 H2Oгаз (1)
(M1)SO4· 6 H2O = (M1)SO4· 5 H2O + H2Oгаз (2)
где М1 и М2 – двухвалентные металлы. Константы равновесий (1) и (2) в области температур 400 – 600 К описываются уравнениями:
KP1 = 156,00 – 77980/Т, бар2,
KP2 = 191,00 – 95450/Т, бар.
В сосуд объемом 8 л при Т = 500 К поместили оба кристаллогидрата в равных количествах 0,01 моля. Опишите равновесное состояние.
96. (4/2-00).* Для систем
CuSO4·5H2O = CuSO4·3H2O + 2H2O,
CuSO4·3H2O = CuSO4· H2O + 2H2O,
CuSO4·H>2 = CuSO4 + H2O
давление насыщенного пара при 50° С равно соответственно 47, 30 и 4,4 торр. В герметичный сосуд небольшого объема поместили 1 моль безводного сульфата меди, откачали и затем стали вводить пары воды при данной температуре. Нарисовать зависимость давления паров воды в системе от количества введенных молей воды. Пояснить приведенный рисунок.
97. (2/Э-97). Оценить степень диссоциации метана в реакции
CH4 = C+ 2H2
при общем давлении 1 атм и температурах 300, 600, 900 и 1200 К, если известны следующие термодинамические параметры:
|
|
|
ρ, |
Ср 298, |
|
|
СН4 (г) С (графит) С (алмаз) Н2 (г) |
– 74,85 0 –1,828 0 |
186,19 5,74 2,368 130,52 |
2,265 3,515
|
35,7 8,5
24,6 |
98. (1/Э-07). В проточный реактор подают метан со скоростью 360 моль/час, в реакторе протекает реакция разложения метана до графита и водорода при давлении 1 атм. Обогрев потока метана и реактора осуществляют при помощи хорошо термоизолированной электропечи. Какую мощность нагрева необходимо поддерживать, чтобы на выходе газ содержал более 90 % H2 ? При оценке используйте данные предыдущей задачи (2/Э-97) и полагайте, что реакция разложения метана протекает до равновесия, а теплоемкости веществ не зависят от температуры.
99. (3/Э-97). Основываясь на данных предыдущей задачи (2/Э-97 и 1/Э-07), вывести уравнение Р-Т кривой сосуществования графита и алмаза. При каких условиях алмаз можно получать прямо из метана?
100. (2/1-95). Константы равновесия последовательной термической дегидратации кристаллогидрата MSO4·2H2O (M - металл)
4·2H2O (тв) ⇔ MSO4·H2O ( тв) + Н2О (г), (1)
4·H2O (тв) ⇔ MSO4 (тв) + Н2О (г), (2)
описываются уравнениями
lgKP1 = 11,0 – 12 ·103/Т,
lg KP2 = 14,0 – 15·103/Т.
Возможно ли достичь состояния, в котором равновесно сосуществуют все три формы соли, если в начале процесса в сухую герметически закупориваемую колбу объемом 10 л вносится 0,005 моля соли в виде дигидрата?
101. (6/1-98). Карбонат кальция в природе существует в двух кристаллических модификациях – кальцит и арагонит. Найдите уравнение кривой сосуществования обеих модификаций, если из справочников известно, что
|
|
|
|
|
| Кальцит арагонит СаО СО2 |
–1206,8 –1207,0 –635,1 –393,5 |
91,7 88,0 38,1 213,7 |
82 82 42 37 |
Какая из этих модификаций наиболее устойчива при Т = 300 К, р = 1 бар? Устойчив ли карбонат кальция к разложению в этих условиях на СаО и СО2, если он находится в сухом воздухе с содержанием СО2 0,5 об. %? При какой температуре он начнет разлагаться при сохранении давления воздуха на уровне 1 бар? Молекулярная масса карбоната кальция равна 100,1.
102. (6/Э-94). Превращение кристаллической модификации углекислого кальция “арагонит” в модификацию “кальцит” при 25 °С сопровождается уменьшением изобарно-изотермического потенциала на 190 кал/моль. При каком давлении при этой же температуре обе формы CaCO3 могут сосуществовать? Известно, что плотность арагонита 2,93 г/см3, а кальцита – 2,71 г/см3.
103. (5/1-99). Определите направление реакции
| ΔD fHо298, |
Sо298, |
сPо298, |
ρ298, |
M, г |
|
| Fe2O3 Fe H2 H2O (г) |
–882,16 0 0 –241,83 |
87,45 27,15 130,52 188,84 |
103,76 24,98 28,83 33,61 |
5,25 7,874 — — |
159,69 55,85 2 18 |
104. (6/1-06). Система состоит из двух замкнутых резервуаров, соединенных небольшой трубкой. Систему вакуумировали, в резервуар (1) поместили 1 моль Na2CO3 и нагрели до 400 K, а в резервуар (2) – 2 моля CaCO3. Парциальное давление паров воды поддерживается равным 1 бар. Объем, не занятый твердыми веществами, в каждом из резервуаров составляет 5 л. Оценить, при какой минимальной температуре резервуара (2) возможно получение питьевой соды.
CaCO3 = CaO + CO2 ΔrGo(T) = – 154,6T + 175800 Дж/моль
2NaHCO3 = Na2CO3 + H2O + CO2 ΔrGo(T) = – 345,4T + 132200 Дж/моль
Ca(OH)2 = CaO + H2O ΔrGo(T) = – 128,4T + 101500 Дж/моль
105. (5/1-05). Известно, что при прокалке на воздухе при высоких температурах оксид кобальта Сo3O4 восстанавливается до СоО. Оценить температуру протекания этого процесса на воздухе, если известны следующие величины, при оценке не учитывать зависимость теплоемкости от температуры.
Вещество |
|
|
|
Оксид кобальта Со3O4 Оксид кобальта СоО Кислород О2 |
–910,0 –237,8 0 |
114,4 52,83 205,0 |
123,1 55,0 28,9 |
106. (3/1-07). Для окисления окиси углерода при 600 оС в реактор загрузили 0,6 моля магнетита Fe3O4, 1,5 моля СО и 0,5 моля СО2. Процесс
Fe3O4 + CO = 3 FeO + CO2,
проведенный при постоянном давлении 5.104
Па, завершился получением равновесного газового раствора, средний молекулярный вес которого оказался равным 36,56. Определите константу равновесия и количество оставшегося магнетита.
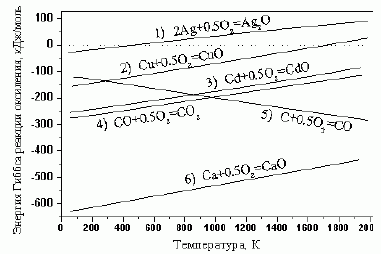
107. (2/1-07). *
Зависимости
*
Зависимости
Определите:
1) при какой T и какие металлы могут самопроизвольно восста-навливаться из соответ-ствующих оксидов;
2) при какой T и какие металлы можно восста-новить монооксидом углерода;
3) при какой T и какие металлы можно восстано-вить графитом? Парциальные давления всех газообразных веществ считать равными 1 атм.
108. (6/1-07). 50 тыс. лет назад на месте современной Аризонской пустыни упал метеорит весом 300 тыс. тонн, а в 1962 году в образовавшемся кратере обнаружили ранее не известную форму SiO2. Используя данные таблицы, предположите, какую кристаллическую фазу SiO2 нашли в кратере, если при столкновении метеорита с Землей давление достигало 1,6·105 атм, а температура – 1300 ºС; МSiO2 = 60 г/моль.
| Модификация SiO2 |
Плотность, |
|
|
|
α-кварц |
2,655 |
–910,7 |
41,5 |
44,6 |
Тридимит |
2,30 |
–905,2 |
41,84 |
44,43 |
Кристобаллит |
2,33 |
–908,0 |
42,6 |
44,56 |
Коэсит |
3,01 |
–905,9 |
40,4 |
45,39 |
Стишовит |
4,35 | –861,5 |
27,8 |
42,97 |
109. (6/1-08). Раздельное окисление СО водяным паром проводят следующим образом. В сосуд, содержащий 2 моля Н2О при 1 атм, помещают порошок металлического Ni массой 0,01 г, дожидаются окончания всех химических превращений. Затем порошок извлекают из 1-го сосуда и помещают во второй сосуд, содержащий 1 моль СО при 1 атм, и также дожидаются окончания всех химических превращений. После чего процедуру повторяют, т. е. порошок периодически приводят в контакт с реагентами в первом и во втором сосудах, в которых поддерживают постоянную температуру 600 К. Найти состав смесей в обоих сосудах после 50-ти повторных циклов. Известны константы равновесия реакций при Т = 600 К:
MNi = 58,69 г/моль