1. ФОРМАЛЬНАЯ КИНЕТИКА
Порядок
реакции
1.4.21. Для реакции орто-пара-превращения
водорода была получена следующая зависимость времени полупревращения от
начального давления орто-водорода:
|
Р0 ×10–4,
Па |
0,67 |
1,33 |
2,67 |
5,33 |
|
t1/2,
мин |
10,8 |
7,5 |
5,3 |
3,7 |
Определите
по этим данным порядок
реакции.
1.4.22. В реакции хлора с водородом время, необходимое
для уменьшения концентрации хлора в 2 раза (t1/2), равно 26 мин при давлении хлора
2 мм рт. ст. и 15 мин при давлении 6 мм рт. ст.
Определите по этим данным порядок реакции
по хлору.
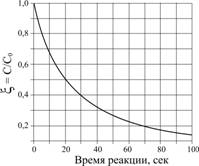
1.4.23. (КР1–2000, № 3). Кинетическая
кривая реакции разложения перекиси
водорода в водном растворе, катализируемая коллоидом гидроксида железа,
представлена на рисунке. С и С0 – текущая и начальная концентрации H2O2, С0 = 0,1 М.
Оцените порядок реакции.
1.4.21. При взаимодействии веществ А и В
образуется окрашенный продукт. Каковы порядки реакции по реагентам, если
начальные скорости роста оптической плотности, измеренные для следующих трёх растворов,
соотносятся как 2,8 : 1 : 0,32.
|
|
Начальные
концентрации |
|
|
[A]0 |
[B]0 |
|
|
Раствор
№ 1 |
10–3 M |
10–1 M |
|
Раствор
№ 2 |
10–3 M |
5 × 10–2 M |
|
Раствор
№ 3 |
10–1
M |
5 × 10–3 M |
1.4.22. (КР1–2001, № 1). При температуре 300 К
происходит образование NOCl из NO и Cl2. В серии опытов были получены следующие значения начальной скорости
образования NOCl:
|
№
опыта |
1 |
2 |
3 |
4 |
5 |
|
PNO,
торр |
80 |
150 |
240 |
240 |
240 |
|
PCl2, торр |
150 |
150 |
150 |
50 |
300 |
|
|
2,3 |
8,1 |
21 |
6,9 |
42 |
Определите
порядок по каждому компоненту и суммарный порядок реакции, полагая, что она
протекает в одну стадию. Оцените время полупревращения для опыта № 2.
1.4.23. (КР1–2002, № 1). При исследовании гидрирования
тиофена водородом (Р = 1 атм) получена следующая зависимость
начальной скорости реакции (М–1с–1) от концентрации
тиофена (моль/л):
|
СТ × 104 |
2,1 |
3,2 |
3,5 |
4,1 |
5,2 |
6,2 |
7,2 |
8,1 |
9,0 |
9,9 |
11,0 |
|
W × 1010 |
2,4 |
3,5 |
4,1 |
4,7 |
5,6 |
6,5 |
7,3 |
7,9 |
8,7 |
9,5 |
10,3 |
Определите порядок реакции по тиофену.
1.4.24. (КР1–2004, № 4). Восстановление NO водородом в
реакторе фиксированного объёма приводит к образованию азота и воды. Если исходные
газы взяты в равных количествах при общем давлении 0,454 атм, то время
полупревращения равно 102 с; если начальное давление было 0,384 атм, то время
полупревращения равно 140 с. Определите порядок реакции.
1.4.25. (КР1–2007, № 2). Рассчитайте наблюдаемый
порядок реакции окисления глюкозы кислородом по данным о зависимости начальной
скорости реакции от начальной концентрации глюкозы. Концентрация кислорода
поддерживается постоянной.
|
C0, М |
0,019 |
0,035 |
0,056 |
0,075 |
0,11 |
0,15 |
0,19 |
0,37 |
|
W0 × 106, М/с |
20 |
21 |
22 |
26 |
29 |
32 |
40 |
44 |
1.4.26. (КР1–2008, № 3). При некоторых условиях продуктом реакции тетрафторэтилена (C2F4) и ацетилена (C2H2) является 1,1-дифторпропин (C3F2H2). В серии опытов с избытком ацетилена начальная концентрация ацетилена выбиралась одинаковой, а начальная концентрация C2F4 варьировалась. Продолжительность реакции во всех случаях была одинакова и равна 0,1 с. По приведённым в таблице данным графически оцените порядок реакции образования C3F2H2 по тетрафторэтилену.
|
[C2F4]
моль/л |
0,0251 |
0,0398 |
0,0631 |
0,1 |
|
[C3F2H2] моль/л |
9,46 × 10–4 |
1,27 × 10–3 |
1,71 × 10–3 |
2,29 × 10–3 |