1. ФОРМАЛЬНАЯ КИНЕТИКА
1.6. Кинетика реакций в открытых системах
1.6.1.
Необратимая
реакция первого порядка A ¾® B происходит в реакторе идеального перемешивания,
степень превращения равна 80 %. Среднее время пребывания реагента в
реакторе равно t. Эту же реакцию проводят в реакторе идеального вытеснения,
время пребывания реагента в реакторе также равно t. Чему равна степень превращения в реакторе
идеального вытеснения?
Решите эту задачу принимая, что степень превращения в
реакторе идеального перемешивания равна: 10 %, 20 %, 30 %,
40 %, 50 %, 60 %, 70 % и 90 %.
1.6.2.
Для
последовательной реакции
A ![]() B
B ![]() C
C
определите максимальную концентрацию промежуточного
вещества [B]max и
необходимое для её достижения время контакта в реакторе идеального смешения,
работающем в стационарном режиме. Сравните полученный результат с выражением
для [B]max для той же
реакции в замкнутой системе.
1.6.3. (Пе1–2006,
№ 2). В
реакторе идеального смешения проводится жидкофазная последовательная реакция
A ![]() B
B ![]() C.
C.
Константы
скорости равны: k1 = 5
мин–1,
k2 = 1,8
мин–1.
Объёмный расход Q смеси равен 300 л/мин, исходная
концентрация вещества А равна 4,8
моль/л, исходные концентрации продуктов В
и С равны нулю. Рассчитайте оптимальный
объём реактора Vopt, позволяющий получить
максимальное количество продукта В в
стационарном режиме.
1.6.4.
При
какой объёмной скорости uo подачи исходного компонента А в реактор идеального смешения можно
ожидать в стационарных условиях получения наибольшего выхода продукта В, если этот продукт получается по схеме
![]() B
B ![]() P.
P.
Объём реактора V, реагент A подаётся в большом избытке инертного
разбавителя.
1.6.5.
При
какой объёмной скорости uo подачи исходного компонента А в реактор идеального смешения можно
ожидать в стационарных условиях получение наибольшего выхода продукта В, если этот продукт получается по схеме
A ![]() 2 B
2 B
![]() P.
P.
Объём реактора V, реагент A подаётся в большом избытке инертного
разбавителя.
1.6.6.
При
какой объёмной скорости uo подачи исходного компонента А в реактор идеального смешения можно
ожидать в стационарных условиях получение наибольшего выхода продукта В, если этот продукт получается по схеме
A ![]() B
B ![]() P
P
Объём реактора V. (Дополнительный вопрос: сопоставить
решение с решением для реактора идеального вытеснения.)
1.6.7.
При
какой объёмной скорости uo подачи исходного компонента А в реактор идеального смешения объёмом
V можно ожидать в стационарных условиях получение наибольшего выхода продукта В, если этот продукт получается по схеме
A ![]() B
B ![]() C
C
1.6.8.
В
реакторе идеального смешения объёмом
Решить задачу для ситуаций, когда исходная смесь: 1)
представляет собой чистый реагент; 2) сильно разбавлена инертным газом.
1.6.9.
В
идеально перемешиваемый растворитель объёма V, химически инертный по отношению
к фенильному свободному радикалу, в течение длительного времени с постоянной
скоростью W0 вводится этот радикал, растворённый в том же
растворителе. При этом общий объём v раствора, введённого за всё время
эксперимента, удовлетворяет условию v << V.
Введённый фенильный радикал рекомбинирует в получающемся более разбавленном
растворе с константой скорости k2, образуя дифенил.
Выведите уравнение, описывающее изменение концентрации
фенильного радикала во времени, и найдите из него характеристическое время
установления стационарной концентрации этого радикала. Начальную концентрацию
радикала примите равной нулю.
1.6.10. В струевом
реакторе длиной
2 CH3CHO ¾® 2 CH4 + 2 CO.
Константа
скорости этой реакции 0,33 М–1×с–1. Определите, какой процент
ацетальдегида окажется разложившимся при скорости его подачи 50 г/ч.
1.6.11. В реакторе полного смешения объёмом
C2H5Br ¾® C2H4 + HBr.
Найдите область температур, при которых будет
происходить 5 % и 50 % разложения бромистого этана, если скорость
подачи 7 л/ч, а константа скорости k = 1013exp(–E/RT) с–1, где E
= 54 ккал/моль.
1.6.12. В реакторе идеального вытеснения при
450 °С и 1 атм происходит разложение метанола
CH3OH ![]() CO
+ 2 H2.
CO
+ 2 H2.
Найдите константу скорости реакции, если глубина пиролиза составляет 75 % при времени контакта t = 1,33 с.
1.6.13. В реактор полного смешения объёмом V подаётся
со скоростью uo смесь двух веществ с концентрациями [A]0 и [B]0.
Между ними в реакторе идёт обратимая реакция
А ![]() В.
В.
Найдите отношение концентраций [A]/[B] в стационарном
режиме работы реактора. Сравните полученный результат с равновесными
концентрациями А и В.
1.6.14. В проточный реактор поступает смесь СО (0,5 атм) и Н2О:
CO +
H2O ![]() CO2 + H2.
CO2 + H2.
Константа равновесия при температуре реактора равна K = 20, а константа скорости k1 равна 10–2 атм–1 с–1.
Время нахождения смеси в реакторе 102 с. Рассчитайте степень
превращения СО и Н2О в СО2 и Н2 в процентах от максимально возможной, определяемой
термодинамическим равновесием.
1.6.15. (Пе1–2003, № 5). Каталитическую реакцию
паровой конверсии
СО +
Н2О ¾® Н2 + СО2
изучают в реакторе идеального вытеснения при давлении
20 атм, температуре 320 °С, загрузке катализатора 0,3 см3,
объёмной скорости подачи исходной газовой смеси 0,6 л н.у./с и
составе: СО – 17 об.%, Н2О – 33 об.%, N2 – 50 об.%. Установлено, что при этих условиях конверсия СО составляет 20 %, реакция
является практически необратимой, характеризуется первым порядком по
концентрации СО и нулевым порядком по
концентрации Н2О. Определите эффективную константу
скорости реакции.
1.6.16. (Пе1–2008, № 2).
В реактор идеального перемешивания
подаётся эквимолекулярная смесь 50 % МеОН + 50 % азота. В реакторе происходит реакция разложения метанола с образованием СО и водорода. Порядок реакции по
метанолу – первый. Температура 400 °С, давление 1 атм, скорость подачи азотно-метанольной
смеси u = 1 л/с, объём реактора
V =
1.6.17. В реакторе периодического действия должна быть
достигнута производительность 50 т/сутки по этилацетату, получаемому из
этилового спирта и уксусной кислоты:
C2H5OH + CH3COOH ![]() CH3COOС2H5 + H2O.
CH3COOС2H5 + H2O.
(А)
(В) (R)
(S)
Скорость
реакции в жидкой фазе
![]() .
.
При 100 °С k = 7,93 × 10–6 м3/(кмоль×с), K = 2,93, в исходной жидкости содержится
23 вес.% кислоты, 16 вес.% спирта и отсутствует эфир. Должна
достигаться степень превращения кислоты – 35 %. Плотность жидкости
примерно постоянна и равна 1080 кг/м3. Реактор будет работать
24 часа в сутки. Время для заполнения, опустошения и пр. составляет в
сумме для подобных реакторов 1 ч. Какой требуется объём реактора?
1.6.18. (Экз–2006, № 1).
В реакторе полного смешения протекает мономолекулярная необратимая реакция:
A ![]() B,
k = 10–2 c–1.
B,
k = 10–2 c–1.
Время контакта реакционной смеси t = 50
с. Первоначально в реактор подают сильно разбавленный инертным газом реагент А с начальной концентрацией 10–3
М до установления стационарной концентрации, а затем концентрацию А в подаваемой смеси скачком уменьшают
до нуля. Найдите концентрации А и B в реакторе через 100 c после
скачкообразного изменения начальной концентрации реагента А.
1.6.19. (КР1–2002, № 4). Реагент B с объёмной скоростью
1 см3/с подаётся в реактор
полного смешения объёмом 1 см3. В реакторе происходит реакция B ® P, константа скорости равна 2 с–1.
Концентрация B0 на входе в реактор изменяется во времени следующим образом:
![]() , b = 0,01 моль/л×с.
, b = 0,01 моль/л×с.
Определите концентрацию на выходе из реактора в
моменты времени t и 2 t, если t = 1/3 с.
1.6.20. Димеризация изопрена (растворённого в большом
количестве инертного разбавителя) изучалась в струевом реакторе идеального
вытеснения объёмом
|
T, K |
550 |
600 |
650 |
700 |
750 |
|
C10H16/C5H8 |
3 × 10–5 |
2,4 × 10–4 |
1,5 × 10–3 |
6,6 × 10–3 |
2,4 × 10–2 |
Определите
по этим данным предэкспоненциальный
множитель и энергию активации константы скорости этой реакции.
1.6.21. (КР1–1997, № 3). Стехиометрическая смесь CO и N2O пропускается через
реактор идеального вытеснения со скоростью ![]() равна 0,46 М–1с–1.
равна 0,46 М–1с–1.
При какой длине реактора концентрации всех компонентов
(CO, CO2,
N2O и N2) на выходе реактора будут одинаковыми?
1.6.22. (КР1–1998, № 4). В реакторе идеального
смешения объёмом
1.6.23. (КР1–2001, № 3). В реакторе полного перемешивания протекают
превращения согласно схеме
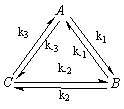
Раствор
реагента А с концентрацией
Покажите,
что k1k2k3 / k–1k–2k–3 = 1, и определите k1 и k–3, если известно, что отношение концентраций B/A на выходе равно 0,5.
Реактор работает в стационарном режиме.
1.6.24. (КР1–2003, № 3). В реактор полного смешения
объёмом
CH3CHO ¾® CH4 + CO
с константой скорости k = 2 × 10–2 c–1. Найдите концентрацию ацетальдегида на выходе из реактора,
предполагая, что реактор работает в стационарном режиме.
1.6.25. (КР1–2003, № 4). Реактор идеального вытеснения
состоит из двух одинаковых ступеней, между которыми имеется теплообменник.
Температура первой ступени 200 °С, температура второй ступени
180 °С.
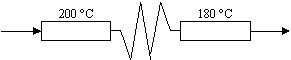
В реакторах идёт реакция изомеризации вещества A ¾® B. Степень превращения
после первой ступени равна 50 %. Чему равна степень превращения на выходе
из реактора, если время контакта одинаково для первой и второй ступеней, а
энергия активации этой реакции равна 100 кДж/моль.
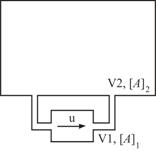
1.6.26. (Экз–2004, № 1). Два реактора полного
перемешивания объёмом V1 и V2 литров соединены так, как показано на рисунке. В
реакторе 1 протекает мономолекулярная реакция превращения газа А в газ B с константой скорости k. Температуры реакторов одинаковы. Найдите зависимость
концентрации А от времени для каждого
из реакторов, если в начальный момент [A]1 = [A]2 = a. Объёмом
соединительных линий пренебречь.
1.6.1.
(КР1–2005,
№ 2). Получение продукта P из реагента A проходит в 2 стадии. На первой стадии чистый
газообразный A подаётся в реактор
полного смешения, в котором происходит реакция (1). Объём реактора
Получившаяся смесь сразу же
подаётся на вход реактора идеального вытеснения (объём
![]() 2)
2) ![]()
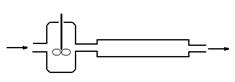
Известно, что k2 =
0,1 × k1.
Определите селективность процесса по продукту Р (отношение количества образовавшегося продукта P
к количеству израсходованного реагента А).
1.6.2. (КР1–2006,
№ 3). Реакцию дегидратации изопропанола
C3H7OH ¾® C3H6 + H2O
проводили в реакторе идеального
вытеснения при постоянном давлении 1 атм. Установлено, что порядок реакции по
изопропанолу равен единице. Если в исходной смеси изопропанол сильно разбавлен
инертным газом, то степень превращения x равна 0,8 при температуре 200 °С.
Объёмная скорость подачи исходной реакционной смеси 0,2 мл/с, объём реактора 1
мл.
Чему
будет равна степень превращения изопропанола, если в реактор подавать чистый
газообразный изопропанол с такой же объёмной скоростью?
1.6.3.
(КР1–2007, № 5). На вход реактора идеального
вытеснения объёмом 250 см3 подаётся реагент A при атмосферном
давлении и температуре 298 K с начальной объёмной
скоростью потока 10 см3/с. В реакторе происходит процесс
![]() B.
B.
Найдите величину константы скорости k, если известно, что на выходе из
реактора скорость потока уменьшается вдвое по сравнению с начальной.
Решите предыдущую задачу, считая что реакция
происходит в реакторе полного перемешивания.
(КР1–2008, № 2). Селективная тетрамеризация этилена в
1-октен проводится в стационарных условиях в реакторе полного перемешивания (в
реактор подаётся газообразный этилен, в результате реакции образуется жидкий
октен). При малых временах контакта t0 степень превращения этилена a линейно
зависит от времени контакта
![]() ,
,
причём коэффициент пропорциональности b не зависит от давления в
реакторе. Определите
порядок реакции по этилену.
1.6.4.
(Экз–2007, № 5). В реакторе полного смешения при
атмосферном давлении протекает метанирование смеси СО и СО2:
1) ![]() ,
,
2) ![]() .
.
Начальные концентрации реагентов
равны: 10 об.% СО, 30 об.% СО2, 60 об.% Н2, метан и вода отсутствуют.
Найдите
концентрации всех веществ на выходе из реактора, если степени превращения СО и СО2
составляют 0,8 и 0,167 соответственно.
1.6.33. В
реакторе идеального вытеснения происходит сложная реакция
A + B ![]() D
D
D ![]() P.
P.
На вход реактора объёма V = 250
мл c объёмной скоростью u0 = 50
мл/мин подаётся реакционная смесь, содержащая реагенты А и В в концентрациях СА0
=
1.6.34. В
реакторе идеального вытеснения происходит реакция
A + B ![]()
На вход реактора объёма V c
объёмной скоростью u0 подаётся реакционная смесь,
содержащая чистые реагенты А и В в равных концентрациях СА0
= СВ0 = а. Найдите зависимость степени превращения реагентов А и В
от объёмной скорости подачи реагентов.
1.6.35. В реакторе
идеального вытеснения происходит реакция
A ![]()
На вход реактора объёма V c
объёмной скоростью u0 подаётся реакционная смесь, содержащая
чистый реагент А в концентрации СА0.
Найдите
зависимость степени превращения реагента от объёмной скорости подачи.