3. КИНЕТИКА СЛОЖНЫХ ХИМИЧЕСКИХ ПРОЦЕССОВ
3.3. Цепные разветвленные процессы
3.3.1. Цепное воспламенение в смесях О2 и Н2 в основных чертах может быть описано механизмом:
0. H2
+ O2 ![]() 2 OH˙, зарождение цепи;
2 OH˙, зарождение цепи;
1. OH˙ + H2 ![]() H2O + H˙, стадия продолжения цепи;
H2O + H˙, стадия продолжения цепи;
2. H˙ + O2 ![]() OH˙ + O˙˙,
стадия разветвления цепи;
OH˙ + O˙˙,
стадия разветвления цепи;
3. O˙˙ + H2 ![]() OH˙ + H˙, стадия продолжения цепи;
OH˙ + H˙, стадия продолжения цепи;
4. H˙ + стенка ![]() гибель, обрыв цепи на стенке;
гибель, обрыв цепи на стенке;
5. H˙ + O2 + M ![]() HO2˙
+ M, обрыв цепи в объеме.
HO2˙
+ M, обрыв цепи в объеме.
Было найдено, что в стехиометрической смеси в сосуде
диаметром 5,8 см, обработанном плавиковой кислотой, при 800 К нижний
предел воспламенения Р1 = 0,1 мм рт. ст.
Эффективность рекомбинации атомов Н
на стенке в таком сосуде e = 10–4.
Получите условие воспламенения. Выясните, в
какой области – диффузионной или
кинетической – проходят реакции
активных частиц для указанных выше условий эксперимента. Определите из этих
данных k2 и верхний предел Р2, считая k6 = 10–32 см6×с–1.
3.3.3. Для механизма, приведённого в задаче 3.3.1,
рассчитайте для стехиометрической смеси и Т = 800 К соотношение
концентраций активных частиц ![]() и
и ![]() в условиях
квазистационарности, приняв, что k1 = 3,7 × 10–11exp(–5240/RT), k3 = 4,1 × 10–11exp(–9840/RT),
k2 = 2,6 × 10–10exp(–16700/RT).
(В экспонентах цифры даны в кал/моль, константы скорости – в
cм3×с–1)
в условиях
квазистационарности, приняв, что k1 = 3,7 × 10–11exp(–5240/RT), k3 = 4,1 × 10–11exp(–9840/RT),
k2 = 2,6 × 10–10exp(–16700/RT).
(В экспонентах цифры даны в кал/моль, константы скорости – в
cм3×с–1)
3.3.4.
Выведите
выражения для концентрации кислорода на нижнем и
верхнем
пределах самовоспламенения для реакции окисления Н2 молекулярным кислородом.
3.3.5.
Как
изменится значение нижнего
предела самовоспламенения смеси водорода с кислородом при разбавлении
инертным газом, если обрыв на стенке протекает в кинетическом режиме?
3.3.6.
Два
сферических сосуда одинакового объёма V соединены трубкой с краном, причем
объём трубки u << V.
В начальный момент времени кран закрыт. В одном из
сосудов находится стехиометрическая смесь Н2 и О2
под давлением, превышающим верхний предел её самовоспламенения в 1,9 раза.
Второй сосуд либо вакуумирован, либо содержит чистый водород, чистый кислород
или чистый гелий при тех же температуре и давлении. Воспламенится ли смесь в
каждом из этих четырех случаев, если открыть кран? Ответ обоснуйте
соответствующими формулами. Указание. При решении принять, что температура
смеси существенно превышает температуру мыса полуострова самовоспламенения.

3.3.7.
Реакция
окисления водорода кислородом в их стехиометрической смеси протекает в
условиях, когда обрыв цепи на стенках реакционного сосуда контролируется
диффузией.
Изменятся ли (и если да, то в какую сторону) нижний и
верхний пределы цепного воспламенения при разбавлении этой смеси аргоном в
соотношении 3 моль Ar на 3 моль
смеси? Ответ обоснуйте.
3.3.8.
Малые
добавки вещества RH в стехиометрическую смесь Н2 и О2
смещают нижний предел самовоспламенения за счёт реакции
![]() (неактивная частица).
(неактивная частица).
1. Оцените константу скорости этой реакции, если при
743 К относительное изменение давления DР/Р для нижнего предела равно 0,05 при PRH/P
» 0,01 (PRH
– парциальное давление RH, Р – общее давление смеси), а константа
скорости реакции
![]()
![]()
![]()
при этой температуре равна 3,3 × 107 М–1с–1.
2. Повысится или понизится нижний предел
самовоспламенения?
3.3.9.
При
добавлении пропана в смесь 4 Н2 + О2,
нижний предел цепного воспламенения повышается за счёт дополнительного обрыва
цепей по реакции
6) ![]() .
.
По приведённым в таблице значениям нижнего
предела воспламенения для чистой смеси (![]() ) и смеси, содержащей 0,5 % С3Н8
(Р1), рассчитайте предэкспоненциальный множитель и энергию активации
реакции 6, приняв для константы скорости реакции
) и смеси, содержащей 0,5 % С3Н8
(Р1), рассчитайте предэкспоненциальный множитель и энергию активации
реакции 6, приняв для константы скорости реакции ![]() значение 2,6 × 10‑10 exp(–E/RT) см3×с–1, где E = 70 кДж/моль. Обрыв цепей протекает в
кинетической области.
значение 2,6 × 10‑10 exp(–E/RT) см3×с–1, где E = 70 кДж/моль. Обрыв цепей протекает в
кинетической области.
|
T,
°C |
580 |
600 |
620 |
640 |
660 |
|
|
6,62 |
5,88 |
5,12 |
4,76 |
4,32 |
|
Р1, торр |
8,37 |
7,30 |
6,26 |
5,65 |
5,05 |
3.3.10.
(КР3–2004,
№ 4). Для смеси 80 % Н2 + 20 % О2 верхний предел
воспламенения при 803 К соответствует давлению
40 мм рт. ст. Введение в смесь 0,5 % этана понижает
величину верхнего предела до
30 мм рт. ст. Определите из этих данных константу скорости
реакции ![]() , если константа скорости реакции
, если константа скорости реакции ![]() равна 1,16 × 10–32 cм6×с–1.
равна 1,16 × 10–32 cм6×с–1.
3.3.11.
С
помощью метода ЭПР измеряли зависимость от
времени концентрации атомов Н· и молекул О2 при реакции кислорода с водородом в условиях,
соответствующих области внутри полуострова воспламенения. Результаты этих
измерений даны в таблице.
|
[O2] × 10–15, см–3 |
4,0 |
3,5 |
3,0 |
2,5 |
2,0 |
1,5 |
1,0 |
|
[Н·] × 10–15, см–3 |
0 |
0,23 |
0,85 |
1,11 |
1,23 |
1,07 |
0,46 |
Определите по этим данным константу скорости реакции разветвления цепи (k2), если обрыв идёт на стенке и константа скорости k4 = 40 с–1 (см. задачу 3.3.1).
3.3.12.
Рассчитайте
координаты (давление и температуру) мыса
полуострова воспламенения стехиометрической смеси водорода с кислородом для
цилиндрического реактора диаметром
![]() и
и
![]()
равны ![]() см3×c–1 и 10–33 см6×c–1.
см3×c–1 и 10–33 см6×c–1.
3.3.13.
(КР3–2004,
№ 5). Рассчитать координаты (давление и температуру) мыса полуострова
самовоспламенения стехиометрической смеси водорода с кислородом для
сферического реактора диаметром
![]() и
и
![]()
равны 10–10 exp(–70 кДж/моль/RT) см3×с–1 и 10–33 см6×с–1 соответственно.
3.3.14. (КР3–2003, № 2). В три одинаковых по размеру, но изготовленных из разного материала цилиндрических сосуда радиусом 2 см напускают стехиометрическую смесь H2 и O2 до концентрации 2,45 × 1015 см–3. В таблице приведены коэффициенты прилипания e для реакции атомов водорода со стенкой.
|
Кварц |
10–3 |
|
Алюминий |
0,1 |
|
Платина |
1 |
Определите, в каком из сосудов смесь взорвётся при более низкой температуре и оцените эту температуру, если взрыв происходит на нижнем пределе самовоспламенения в условиях кинетически контролируемого обрыва цепи.
Константа скорости
элементарной реакции ![]() составляет 1,5 × 1011 × exp(–70 кДж/моль/RT) M–1с–1.
составляет 1,5 × 1011 × exp(–70 кДж/моль/RT) M–1с–1.
3.3.15.
(Пе1–2008, № 4). Нижний предел
самовоспламенения стехиометрической смеси водорода с кислородом в сосуде
диаметром
3.3.16.
(КР3–2007, №5). В цилиндрическом реакторе радиусом
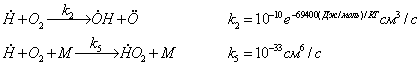
Оцените, на сколько повысится температура мыса полуострова самовоспламенения,
если диаметр реактора уменьшить в 10 раз.